Genome-Nanostructures
Lichtmikroskop enthüllt dreidimensionale Genomstruktur
Mit speziellen Tricks konnten Wissenschaftler die Auflösung von Lichtmikroskopen drastisch verbessern. Dadurch schafften sie es, an intakten Zellkernen Strukturdetails der Chromosomen mit fast molekularer Auflösung zu ermitteln.
Von Georg Wolschin
Ein Bild sagt bekanntlich mehr als tausend Worte. Das gilt auch für biologische Strukturen. Wenn man sie nur detailliert genug betrachten kann, springen viele Aspekte ihrer Funktion unmittelbar ins Auge. Den ersten Einblick in die Feinstruktur von Lebewesen eröffnete das Lichtmikroskop. Mit ihm konnten schon in den dreißiger Jahren des 19. Jahrhunderts erstmals Zellen und mit geeigneten Färbungstechniken wenig später auch der Zellkern sowie _ zunächst nur bei Zellteilungen _ die Chromosomen sichtbar gemacht werden. Inzwischen wissen wir, dass die menschliche Erbinformation auf 46 Chromosomen in den Zellkernen gespeichert ist und etwa sieben Milliarden "Buchstaben" umfaßt, in denen die Bauanleitungen für 300 Millionen Proteine verschlüsselt sind.
Derzeit geht das Human Genome Project, ein internationaler Kraftakt zur vollständigen Entzifferung des menschlichen Genoms, in den Schlußspurt (siehe Spektrum der Wissenschaft, 3/2000, S. 24). Spätestens bis zum Jahr 2002 soll die Abfolge sämtlicher Buchstaben des genetischen Alphabets _ der "Basen" A (Adenin), C (Cytosin), G (Guanin) und T (Thymin) _ vorliegen. Doch damit wird die Erbinformation noch keineswegs auch entschlüsselt sein: Für weite Passagen bleibt die Bedeutung des "Textes" zunächst unklar.
Hinzu kommt, daß in der Abfolge der Buchstaben allein vermutlich nicht die gesamte Information steckt, die eine Zelle zum Funktionieren braucht. Durch Wechselwirkung mit Proteinen und Ionen nimmt das fadenförmige Erbmolekül DNA innerhalb eines Chromosoms eine komplizierte dreidimensionale Gestalt an. Vieles deutet darauf hin, dass diese räumliche Struktur von großer funktioneller Bedeutung ist. Beispielsweise dürfte sie entscheidend mitbestimmen, welche Gene zu einem bestimmten Zeitpunkt gerade abgelesen werden. Bisher ließ sie sich mit lichtmikroskopischen Methoden allerdings nicht scharf genug abbilden.
Das liegt an der mangelnden Ortsauflösung von Lichtmikroskopen, die normalerweise durch zwei Faktoren begrenzt ist: die Wellenlänge des verwendeten Lichtes und die Apertur, gleichsam der Blickwinkel, des Mikroskops. Beim technisch maximal möglichen Aperturwinkel (Bild 1) von 70 Grad ist das Beugungs-Hauptmaximum _ und damit der Brennpunkt des Mikroskops _ ungefähr 200 Nanometer breit und 600 bis 700 Nanometer lang.
Daß die Auflösung entlang der optischen Achse drei- bis viermal schlechter ist als in der Brennebene, liegt am begrenzten Aperturwinkel: Nur wenn er 360 Grad betrüge, hätte die fokussierte Welle Kugelform, und die Auflösung wäre in allen Raumrichtungen gleich gut. Mittlere Abstände zwischen funktionell bedeutsamen Genomstrukturen _ beispielsweise Genen _ und der Oberfläche von Chromosomen können wesentlich kleiner sein als 600 Nanometer. Deshalb lässt sich die dreidimensionale Feinstruktur der Chromosomen mit konventioneller optischer Mikroskopie nicht erforschen.
Allerdings sind in neuerer Zeit Methoden entwickelt worden, die Ortsauflösung optischer Mikroskope über den "naturgegebenen" Wert zu steigern. So gelang es jüngst einer Arbeitsgruppe um Stefan Hell am Max-Planck-Institut für biophysikalische Chemie in Göttingen, durch geeignete Überlagerung zweier gegeneinander laufender Wellenfronten die Apertur des Mikroskops so zu erhöhen, dass sich fast die gleiche Auflösung erzielen lässt wie bei einem "idealen" Instrument mit voller Apertur (Bild 1 unten).
Der drei- bis viermal schärfere Fokus entlang der optischen Achse ermöglicht es zum Beispiel, in Aufnahmen einer Mauszelle fluoreszenzmarkierte Mikrotubuli _ röhrenförmige Streben des Fasergerüsts, das der Zelle Form und Festigkeit gibt _ zu unterscheiden, die bisher nicht zu trennen waren (Bild 2). Die Lichtwellenlänge beträgt 780 Nanometer, die laterale Auflösung 210 und die axiale 145 Nanometer. Man bezeichnet die neue Anordnung als 4Pi-konfokales Mikroskop, da der volle Raumwinkel 4pi beträgt. Bearbeitet man die Aufnahmen zusätzlich mit mathematischen Methoden der Bildrestaurierung, wird dieses Gerät zum höchstauflösenden fokussierenden Lichtmikroskop, das es derzeit gibt.
Ganz neue Möglichkeiten zur Gewinnung optischer Information eröffnen selbstleuchtende Objektpunkte. Der geometrische Ort einer solchen Lichtquelle _ etwa eines fluoreszenzmarkierten Gens im Zellkern _ wird durch das Maximum der Intensitätsverteilung ihres Beugungsbildes bestimmt. Mit Verfahren der digitalen Bildverarbeitung lässt er sich mit einer Präzision bestimmen, die wesentlich besser als das Auflösungsvermögen von Hochleistungsmikroskopen ist. Verwendet man beispielsweise fluoreszierende Mikropartikel und konfokale Laserscanningmikroskope, ist eine Ortsbestimmung auf bis zu zehn Nanometer genau erreichbar _ etwa ein Fünfzigstel der benutzten Anregungswellenlänge. Mit anderen neu entwickelten Methoden läßt sich die Position sogar noch präziser ermitteln.
Befinden sich nun zwei kleine selbstleuchtende Objekte unterschiedlicher spektraler Signatur _ beispielsweise zwei verschiedene Gene, die mit zwei unterschiedlichen Fluoreszenzmarkierungen versehen wurden _ dicht beieinander, so kann man die von ihnen erzeugten Beugungsbilder samt den zugehörigen Positionen im dreidimensionalen Raum jeweils gesondert mit einer Genauigkeit von zehn Nanometern lokalisieren. Daraus ergibt sich bei sorgfältiger Kalibrierung auch der Abstand zwischen ihnen mit einer entsprechend hohen Präzision. Dieses Verfahren der spektralen Präzisionsdistanz- Mikroskopie (SPDM) hat eine Gruppe um Christoph Cremer am Kirchhoff-Institut der Universität Heidelberg entwickelt und zum Patent angemeldet. Damit lassen sich zwei Objekte unterschiedlicher spektraler Signatur noch im Abstand von 30 Nanometern in beliebiger räumlicher Lage auflösen _ das ist etwa ein Siebzehntel der Anregungswellenlänge.
Ersten Messungen zufolge eignet sich das SPDM-Konzept in der Tat dazu, die dreidimensionale Nanostruktur des Genoms zu erforschen. Mit diesem Verfahren konnten sogar schon Modelle der Genaktivierung experimentell getestet werden. Beispielsweise vermuten Biologen, dass "angeschaltete" Gene, deren Information gerade abgelesen wird, sich an der Oberfläche des kompliziert gefalteten Chromosomenstrangs befinden. Wenn sie "abgeschaltet" werden, müßte sich die dreidimensionale Struktur des betreffenden Chromosomenabschnittes lokal derart ändern, daß die Erbinformation ins Innere zu liegen kommt und damit für bestimmte Proteine unzugänglich wird.
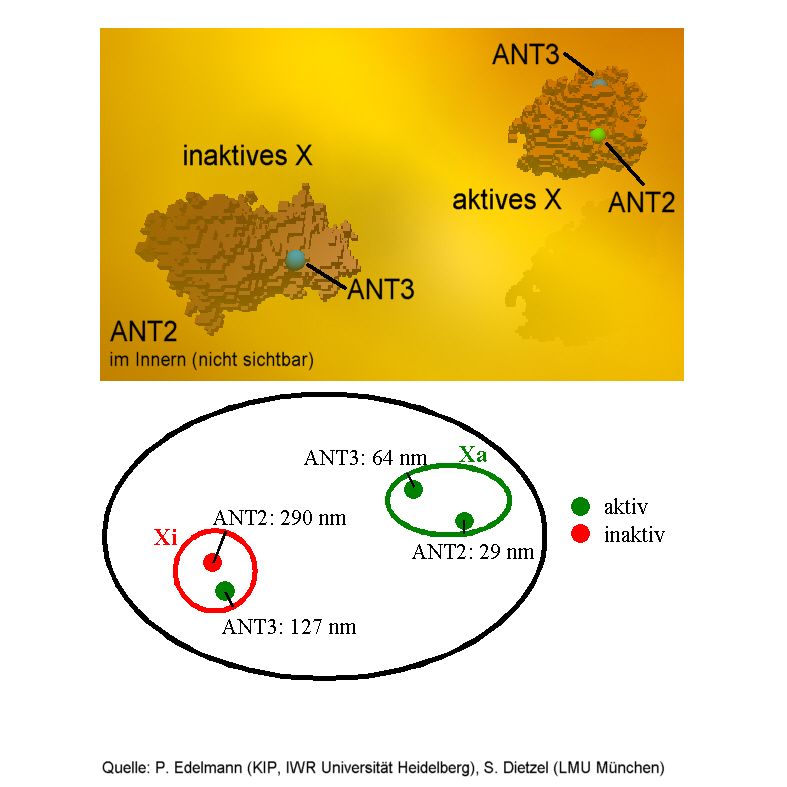
Messungen am Gen für ein bestimmtes Enzym _ die Adenin- Nucleotid-Translocase (ANT) _ haben dies bestätigt. Dieses Gen befindet sich in zwei Varianten (ANT2/ANT3) auf dem weiblichen Geschlechtschromosom, dem sogenannten X- Chromosom. Christoph Cremer und seine Mitarbeiter bestimmten nun per SPDM die Position dieser beiden Gen- Varianten im an- und abgeschalteten Zustand relativ zur Oberfläche des X-Chromosoms. In der Tat zeigte sich, daß die Variante, die nicht abgelesen wurde, um etwa 260 Nanometer ins Innere des Chromosomens verschoben war (Bild 3).
Solche Erfolge sind Ansporn, das Verfahren weiter zu verbessern. Insbesondere wollen die Heidelberger Wissenschaftler umfassendere multispektrale Markierungsmethoden entwickeln, um möglichst viele Objekte (DNA- und RNA-Sequenzen, Proteine) im Beobachtungsvolumen unterscheiden zu können. Zugleich soll die dreidimensionale Auflösung (also der kleinste mit SPDM unterscheidbare Abstand) auf wenige Nanometer gesteigert werden. Aus theoretischen Gründen setzt dies voraus, daß zugleich der kleinste unterscheidbare Abstand zwischen Punkten derselben spektralen Signatur verringert wird. Daher sind auch für die SPDM jene Methoden zur Verbesserung der Ortsauflösung sehr wichtig, welche die Göttinger Gruppe entwickelt hat _ weshalb sich beide Forschungsrichtungen in idealer Weise ergänzen. Langfristiges Ziel ist es, in konservierten Zellkernen die Genomstruktur auf der Größenskala einzelner Nucleosomen zu untersuchen. (Nucleosomen sind Protein-"Spulen", auf die jeweils etwa zwei Windungen des DNA-Fadens gewickelt sind.) Gleichzeitig müssen neue Markierungstechniken entwickelt werden, die mit der weiter verbesserten Auflösung Schritt halten. Inzwischen ist es bereits gelungen, einzelne Chromosomenabschnitte in lebenden Zellen zu markieren.
Bild 1: Durch die Beugung im Objektiv des Mikroskops wird die Lichtwelle in ein entlang der optischen Achse ausgedehntes Intensitätsmaximum (orange) fokussiert; seine Ausdehnung bestimmt die Auflösung (oben). Durch eine gegenüberliegende zweite Wellenfront erhält man bei konstruktiver Interferenz im 4Pi-konfokalen Mikroskop ein wesentlich engeres Maximum (die Seitenmaxima werden entfernt) und entsprechend bessere Auflösung.
((Quelle: MPG-Jahrbuch 1999, Seite 134; Bildnachweis: S. Hell und M. Nagorni, MPI für Biophysikalische Chemie, Göttingen 1999))
Bild 2: Mikroskopaufnahmen fluoreszenzmarkierter Mikrotubuli einer Maus-Fibroblast-Zelle an derselben Stelle mit (a) einem üblichen konfokalen Mikroskop (Wellenlänge 780 Nanometer), (b) mit dem 4Pi-konfokalen Mikroskop, das vierfach bessere Auflösung entlang der optischen Achse ermöglicht.
((Quelle: MPG-Jahrbuch 1999, Seite 136; Bildnachweis: S. Hell et al., MPI für Biophysikalische Chemie, Göttingen 1999))
Bild 3: Mit spektraler Präzisionsdistanz-Mikroskopie (SPDM) lässt sich die Verschiebung transkriptionsinaktiver Gene ins Innere der Chromosomenterritorien (hier beim X- Chromosom) nachweisen. Oben: Darstellung einer konfokalen Laserscanningmikroskop-Aufnahme eines menschlichen Zellkerns. Rechts das insgesamt genetisch aktive weibliche X-Chromosom (Xa); links das genetisch inaktive X-Chromosom (Xi). Die Positionen der Gene ANT2 und ANT3 sind jeweils rot und gelb angegeben. Unten: Schematische Darstellung der mit SPDM in 42 Kernen vermessenen mittleren Abstände der genetisch aktiven (grün) und des inaktiven Gens (rot) von der Chromosomenoberfläche.

((Quelle: P.Edelmann, S.Dietzel, C. Cremer, T. Cremer; Kirchhoff-Institut der U Heidelberg und LMU München)).
siehe Spektrum d. Wissenschaft 9 (2000) 22 für den vollständigen illustrierten Artikel.